Аденозинтрифосфат (АТФ) – определение, структура и функции
Определение аденозинтрифосфата
Аденозинтрифосфат, также известный как АТФ, является молекула который несет энергию внутри клеток. Это основная энергетическая валюта клетка и является конечным продуктом процессов фотофосфорилирования (добавление фосфатная группа к молекуле, использующей энергию света), клеточное дыхание, а также ферментация, Все живые существа используют АТФ. Помимо использования в качестве источника энергии, он также используется в передача сигнала пути для клеточной коммуникации и включается в дезоксирибонуклеиновую кислоту (ДНК) во время синтеза ДНК.
Структура АТФ
Функции АТФ
Источник энергии
АТФ является основным носителем энергии, которая используется для всех клеточных активностей. Когда АТФ гидролизуется и превращается в аденозиндифосфат (АДФ), выделяется энергия. Удаление одной фосфатной группы высвобождает 7,3 килокалорий на моль или 30,6 кДж на моль при стандартных условиях. Эта энергия питает все реакции, которые происходят внутри клетки. АДФ также может быть преобразован обратно в АТФ, так что энергия доступна для других клеточных реакций.
АТФ производится несколькими различными способами. Фотофосфорилирование – это метод, специфичный для растений и цианобактерий. Это создание АТФ из АДФ с использованием энергии солнечного света, и происходит во время фотосинтез, АТФ также образуется из процесса клеточного дыхания в митохондрии клетки. Это может быть через аэробного дыхания, который требует кислорода, или анаэробное дыхание, чего нет. Аэробного дыхания производит АТФ (наряду с углекислым газом и водой) из глюкозы и кислорода. Анаэробное дыхание использует химические вещества, кроме кислорода, и этот процесс в основном используется археями и бактерии которые живут в анаэробных условиях. Ферментация является еще одним способом получения АТФ, который не требует кислорода; он отличается от анаэробного дыхания, потому что он не использует цепь переноса электронов, Дрожжи и бактерии являются примерами организмов, которые используют ферментацию для образования АТФ.
Передача сигнала
АТФ является сигнальной молекулой, используемой для клеточной коммуникации. Киназы, которые являются ферментами, которые фосфорилируют молекулы, используют АТФ в качестве источника фосфатных групп. Киназы важны для передачи сигнала, то есть как физический или химический сигнал передается от рецепторов снаружи клетки внутрь клетки. Как только сигнал находится внутри ячейки, ячейка может ответить соответствующим образом. Клеткам могут быть даны сигналы расти, метаболизироваться, дифференцироваться в определенные типы или даже умирать.
Синтез ДНК
Нуклеиновая основа аденина является частью аденозина, молекулы, которая образуется из АТФ и помещается непосредственно в РНК. Другие нуклеиновые основания в РНК, цитозине, гуанине и урациле, аналогично образуются из CTP, GTP и UTP. Аденин также обнаружен в ДНК, и его включение очень похоже, за исключением того, что АТФ превращается в форму дезоксиаденозинтрифосфата (dATP), прежде чем стать частью цепи ДНК.
АТФ, АДФ, АМФ, цАМФ
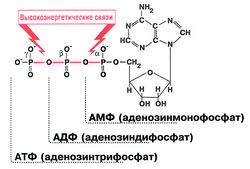
Другие молекулы связаны с АТФ и имеют сходные названия, такие как аденозиндифосфат (АДФ), аденозинмонофосфат (АМФ) и циклический АМФ (цАМФ). Чтобы избежать путаницы, важно знать некоторые различия между этими молекулами.
Аденозиндифосфат (ADP), который иногда также известен как аденозин пирофосфат (APP), особенно в химии, уже упоминался в этой статье. Он отличается от АТФ, потому что он имеет две фосфатные группы. АТФ становится АДФ с потерей фосфатной группы, и эта реакция высвобождает энергию. Сам ADP формируется из AMP. Цикл между АДФ и АТФ во время клеточного дыхания дает клеткам энергию, необходимую для осуществления клеточной деятельности
Аденозинмонофосфат (AMP), также называемый 5′-адениловой кислотой, имеет только одну фосфатную группу. Эта молекула находится в РНК и содержит аденин, который является частью генетический код, Он может быть получен вместе с АТФ из двух молекул АДФ или путем гидролиза АТФ. Это также сформировано, когда РНК сломана. Он может быть преобразован в мочевую кислоту, которая является компонентом мочи, и выводится через мочевой пузырь.
лагерь
Циклический аденозинмонофосфат (цАМФ) происходит от АТФ и является еще одним мессенджером, используемым для передачи сигнала и активации определенных протеинкиназ. Это можно разбить на AMP. Пути цАМФ могут играть роль в некоторых раковых заболеваниях, таких как карцинома, У бактерий он играет роль в обмене веществ. Когда бактериальная клетка не производит достаточно энергии (например, из-за недостатка глюкозы), возникают высокие уровни цАМФ, и это включает гены, которые используют источники энергии, отличные от глюкозы.
- Клеточное дыхание – Энергия из питательных веществ преобразуется в АТФ.
- Передача сигнала – передача сигналов снаружи клетки внутрь.
- Гидролиз – Разрыв связи в молекуле и расщепление ее на более мелкие молекулы в результате реакции с водой.
- киназа – Фермент, который переносит фосфатную группу из АТФ в другую молекулу.
викторина
1. Как можно получить АТФ?A. ФерментацияB. Клеточное дыханиеC. фотофосфорилированияD. Все вышеперечисленное
Ответ на вопрос № 1
D верно. АТФ может быть получен с помощью всех этих методов, хотя разные организмы используют разные методы для его производства и не используют все три из этих методов. Вариант B, клеточное дыхание, включает аэробное и анаэробное дыхание.
2. Где производится АТФ в клетке?A. МитохондрииB. ядроC. РибосомыD. Эндоплазматическая сеть
Ответ на вопрос № 2
верно. АТФ производится в митохондриях, которые являются органеллами в клетке, где происходит клеточное дыхание. Вот почему митохондрии часто называют «электростанцией клетки».
3. В каком типе генетического материала обнаружен аденин?A. ДНКB. РНКC. И ДНК, и РНКD. Ни ДНК, ни РНК
Ответ на вопрос № 3
С верно. Аденин находится как в ДНК, так и в РНК. В ДНК аденин связывается с тимин в то время как в РНК аденин связывается с урацилом. Когда аденин присоединяется к рибозному сахару, он образует аденозин, который является частью АТФ. Аденозин – это молекула, содержащая аденин в РНК, тогда как в ДНК эта молекула представляет собой дезоксиаденозин (аденин, присоединенный к дезоксирибоза сахар).
Синтез АТФ
Содержание
- 1 Анаэробный синтез АТФ: субстратное фосфорилирование, синтез АТФ из фосфокреатина, аденилаткиназная реакция
- 1.1 АТФ (аденозинтрифосфат): молекула, обеспечивающая энергией живые клетки
- 1.2 Синтез АТФ путем субстратного фосфорилирования
- 1.3 Получение АТФ из фосфокреатина
- 1.4 Креатин выводится в форме креатинина
- 1.5 Прием креатина повышает работоспособность
- 1.6 Образование АТФ из АДФ под действием аденилаткиназы
- 2 Аэробный синтез АТФ
- 2.1 Синтез АТФ в дыхательной цепи путем окислительного фосфорилирования
- 2.1.1 Митохондрия
- 2.1.2 Дыхательная цепь
- 2.2 Патологии митохондрий
- 2.2.1 Атрофия зрительного нерва Лебера
- 2.2.2 Митохондриальная энцефаломиопатия, лактацидоз и инсультоподобные эпизоды (синдром MELAS)
- 2.2.3 Болезнь Ли
- 2.1 Синтез АТФ в дыхательной цепи путем окислительного фосфорилирования
- 3 Биосинтез АТФ путем окислительного фосфорилирования (часть I)
- 3.1 Комплекс I
- 3.2 Комплекс II
- 3.3 Комплекс III
- 3.4 Комплекс IV
- 3.5 АТФ-синтаза (комплекс V)
- 3.6 Утечка электронов приводит к образованию активных форм кислорода
- 3.7 Дыхательные яды
- 4 Биосинтез АТФ путем окислительного фосфорилирования (часть II)
- 5 Источники
Анаэробный синтез АТФ: субстратное фосфорилирование, синтез АТФ из фосфокреатина, аденилаткиназная реакция [ править | править код ]
АТФ (аденозинтрифосфат): молекула, обеспечивающая энергией живые клетки [ править | править код ]
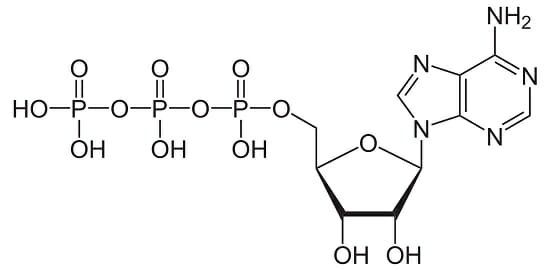
Молекулы АТФ жизненно необходимы. АТФ служит источником энергии, необходимой для сокращения мышц, проведения нервного импульса, протекания многих биохимических реакций и т.п. В покое расходуется 28 г (1 унция) АТФ в минуту, что эквивалентно 1,4 кг (3 фунта) в час, а при физической нагрузке расход АТФ достигает 0,5 кг в минуту! АТФ состоит из аденина, рибозы и трех фосфатных групп, которые называются а-, β- и у-фосфатными группами (рис. 10.1). Гидролиз высокоэнергетических фосфоангидридных связей между β- и у-атомами фосфора или между а- и β-атомами фосфора высвобождает энергию, необходимую для проведения биохимических реакций, т.е. для поддержания жизни организма.
Самый энергетически выгодный метод синтеза АТФ — это аэробное окислительное фосфорилирование. Однако АТФ может также образоваться в анаэробных условиях, хотя и с меньшей эффективностью. Существует три способа анаэробного синтеза АТФ: субстратное фосфорилирование, образование АТФ из фосфокреатина и в результате аденилаткиназной реакции. Хотя анаэробный синтез АТФ и не так энергетически выгоден, способность синтезировать АТФ в бескислородной среде может иметь жизненно важное значение.
Синтез АТФ путем субстратного фосфорилирования [ править | править код ]
На рис. 10.2 показано, что АТФ образуется в процессе гликолиза в ходе фосфоглицераткиназной и пируваткиназной реакций, а также в цикле Кребса в ходе реакции, катализируемой ферментом сукцинил-КоА-синтетазой с участием нуклеозидцифосфаткиназы (рис. 10.3). Примечание: для этих реакций кислород не требуется.

Рис. 10.2. Образование АТФ в ходе гликолиза путем субстратного фосфорилирования

Рис. 10.3. В цикле Кребса путем субстратного фосфорилирования образуется ГТФ, который затем под действием нуклеозиддифосфаткиназы превращается в АТФ
Получение АТФ из фосфокреатина [ править | править код ]
Фосфокреатин — это «аварийный запас» высокоэнергетического фосфата, который можно использовать для быстрого образования АТФ, необходимого для сокращения мышц в анаэробных условиях. Этот интенсивный механизм синтеза АТФ может в экстренных ситуациях спасти жизнь; однако запасы фосфокреатина расходуются очень быстро, всего за несколько секунд.
В периоды покоя, когда молекул АТФ много, креатинкиназа фосфорилирует креатин с образованием фосфокреатина. Особенно важна роль этой реакции в мышцах. Если вдруг требуется сделать резкий рывок, фосфокреатин фосфорилирует АДФ до АТФ, необходимого для сокращения мышц (рис. 10.4) По этой причине фосфокреатин еще называют «фосфаген».

Креатин выводится в форме креатинина [ править | править код ]
Креатин — это аминокислота, не входящая в состав белков. Креатин синтезируется из аргинина и выводится с мочой в форме креатинина. Уровень креатинина в крови и клиренс креатинина используются для оценки скорости клубочковой фильтрации при нарушении работы почек. Примечание: не путайте креатин, креатинин и карнитин.
Прием креатина повышает работоспособность [ править | править код ]
Эргогенные средства — это вещества, которые повышают скорость, силу или выносливость спортсмена. Многие из них опасны и запрещены к использованию. Мнения противоречивы, тем не менее многие ученые сходятся на том, что креатин — единственное эргогенное средство, для которого научно доказано его свойство повышать работоспособность как при спринтерских, так и при продолжительных нагрузках.
Образование АТФ из АДФ под действием аденилаткиназы [ править | править код ]
После того как АТФ гидролизуется для высвобождения энергии, необходимой для сокращения мышц, в клетках образуется и накапливается АДФ. Но АДФ тоже содержит энергоемкую а-фосфоангидридную связь (рис. 10.1). Природа изобретательна: эта энергия становится доступной после того, как в анаэробных условиях две молекулы АДФ под действием аденилаткиназы образуют АТФ (рис. 10.5) (раньше фермент аденилаткиназу называли миокиназой).

Аэробный синтез АТФ [ править | править код ]
Синтез АТФ в дыхательной цепи путем окислительного фосфорилирования [ править | править код ]
Митохондрия [ править | править код ]
Митохондрия — это органелла, по размеру сопоставимая с бактериальной клеткой. Примечательно, что у митохондрии есть две мембраны. Наружная мембрана пронизана молекулами порина. Порины образуют каналы, по которым через мембрану могут проходить молекулы с массой менее 10 кДа. Внутренняя мембрана ПРАКТИЧЕСКИ непроницаема; она образует впячивания — кристы. Через внутреннюю мембрану свободно проходят только небольшие молекулы — вроде Н20 и NH3. Лишь немногие другие молекулы с помощью белков-переносчиков и челночных систем способны преодолеть этот барьер.
Считается, что митохондрия — пример эндосимбиоза. Внутренняя мембрана митохондрии с заключенным в ней содержимым когда-то была древней анаэробной бактерией, которая проникла в примитивную клетку на ранних этапах эволюции. Сохранились и следы прошлого: так, митохондрия имеет свою собственную ДНК (мтДНК), кодирующую 37 генов. 24 из них участвуют в трансляции мтДНК, остальные кодируют белки дыхательной цепи. Примечательно, что только 13 из всех белков митохондриальной дыхательной цепи (а всего их более 85) закодированы в мтДНК. Остальные кодирует ядерная ДНК, и они транспортируются в митохондрию из цитоплазмы.
Дыхательная цепь [ править | править код ]
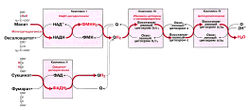
Дыхательная цепь — эффективный путь получения АТФ с использованием НАДН и ФАДН2, которые образуются в процессе окисления метаболического «топлива» [прежде всего углеводов и жирных кислот]. Дыхательная цепь состоит из пяти комплексов — I, II, III, IV и сложного комплекса грибовидной формы (комплекс V). Грибовидный «мультикомплекс» состоит из субъединиц F1 (субъединица «один») и F0 (субъединица «О», связывает олигомицин). Некоторые из комплексов дыхательной цепи содержат цитохромы, которые транспортируют электроны по цепи: комплекс III содержит цитохром b, а комплекс IV — цитохром а/аЗ. Кроме того, в транспорте электронов принимают участие убихинон (кофермент Q10) и цитохром С. Все комплексы дыхательной цепи расположены во внутренней мембране митохондрий. Комплексы I, III и IV не только переносят электроны, но также выполняют функцию молекулярных протонных насосов: они «выкачивают» протоны из матрикса в межмембранное пространство. Внутренняя мембрана непроницаема, в частности, она непроницаема для протонов, поэтому они возвращаются в матрикс только одним путем — через протонный канал комплекса F1/F0, который в этот момент синтезирует АТФ.
Поток электронов упрощенно показан на рис.
Патологии митохондрий [ править | править код ]
Существуют различные нарушения дыхательной цепи. Многие из них наследственно передаются по материнской линии, поскольку все митохондрии зиготы происходят из митохондрий яйцеклетки. При делении клетки тысячи молекул мтДНК случайным образом распределяются между дочерними клетками, поэтому разные ткани могут содержать как нормальные, так и мутантные молекулы мтДНК (это состояние называется гетероплазмией). Вследствие этого клиническая картина при таких патологиях очень изменчива. Мутации в ядерных генах, кодирующих белки дыхательной цепи, передаются по аутосомному типу и обычно вызывают более тяжелые нарушения.
Атрофия зрительного нерва Лебера [ править | править код ]
Атрофия зрительного нерва Лебера вызывается мутацией участка митохондриальной ДНК, который кодирует одну из субъединиц комплекса I. От этого нарушения дыхательной цепи митохондрий сильнее всего страдает, по-видимому, зрительный нерв. Болезнь проявляется во взрослом возрасте и приводит к потере зрения.
Митохондриальная энцефаломиопатия, лактацидоз и инсультоподобные эпизоды (синдром MELAS) [ править | править код ]
Причина синдрома MELAS — мутация гена мтДНК, кодирующего лейциновую транспортную РНК митохондрий. Эта мутация влияет на трансляцию мтДНК, и поэтому при синдроме MELAS нарушена структура всех комплексов дыхательной цепи, кроме комплекса II, который полностью кодируется ядерным геномом.
Болезнь Ли [ править | править код ]
Болезнь Ли — дегенеративное заболевание центральной нервной системы с характерными патологическими изменениями. Обычно развивается в раннем возрасте. Заболевание генетически гетерогенно: чаще всего причиной болезни являются мутации участков ядерных геномов, кодирующих компоненты дыхательной цепи, однако в некоторых случаях болезнь Ли развивается из-за мутаций митохондриальных генов. При болезни Ли может быть нарушена активность АТФ-синтетазы (комплекса V) или комплексов I, II, III, IV. При некоторых формах болезни Ли имеют место нарушения активности пируватдегидрогеназного комплекса.
Недостаточность пируватдегидрогеназного комплекса приводит к повышению в крови концентраций пирувата, лактата и аланина. У некоторых больных наблюдается улучшение состояния при приеме липоевой кислоты или тиамина (коферментов пируватдегидрогеназного комплекса). С ограниченным успехом применяется лечение кетогенной низкоуглеводной диетой. (Кетоновые тела легко проходят гематоэнцефалический барьер, и при их катаболизме образуется ацетил-КоА независимо от пируватдегирогеназного комплекса.)
Биосинтез АТФ путем окислительного фосфорилирования (часть I) [ править | править код ]
Биосинтез АТФ в дыхательной цепи, в котором принимает участие как поток электронов (е-), так и поток протонов (Н+), происходит путем окислительного фосфорилирования. Дыхательная цепь состоит из четырех комплексов (I, II, III, IV) и структуры грибовидной формы — АТФ-синтаза с субъединицами F0/F1 или комплекса V, который синтезирует АТФ из АДФ и неорганического фосфата (Фн). Ниже будет рассмотрено, как создается поток электронов и протонов в дыхательной цепи: первый начинается от комплекса I, второй — от комплекса II. 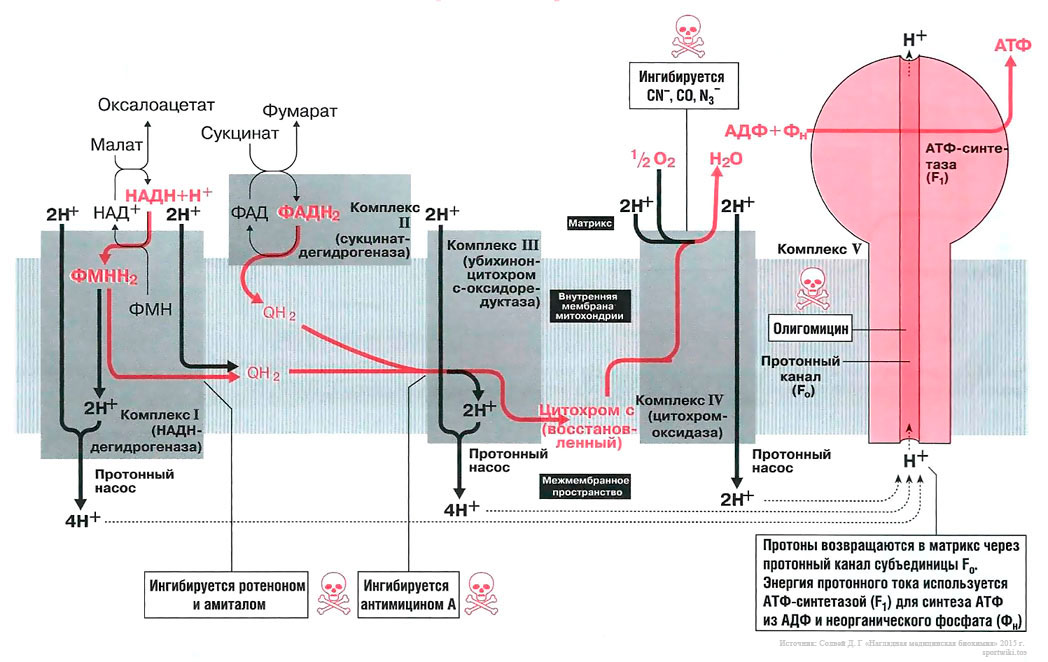
Комплекс I [ править | править код ]
Поток электронов начинается от НАДН. Энергия для синтеза АТФ возникает благодаря разделению зарядов в комплексе I, которое вызывает движение электронов (электрический ток) и протонов (протонный ток). Молекулярный насос комплекса I выкачивает четыре протона в межмембранное пространство. Другие комплексы (III и VI) тоже выкачивают протоны в межмембранное пространство, и образуется электрохимический градиент протонов; в конечном итоге все эти протоны возвращаются обратно через протонный канал АТФ-синтазы (см. ниже). В комплексе I электроны переносятся с НАДН на убихинон (кофермент Q). Два электрона и два протона восстанавливают убихинон до убихинола (QH2), и убихинол движется в толще мембраны к комплексу III.
Комплекс II [ править | править код ]
Поток протонов начинается от ФАДН2. Комплекс II содержит ФАД в виде простетических групп нескольких дегидрогеназ (например, сукцинатдегидрогеназы). Этот ФАД восстанавливается до ФАДН2. Далее комплекс II передает электроны убихинону (Q) для последующего переноса электронов к комплексу III. Примечание, комплекс II не выкачивает протоны.
Комплекс III [ править | править код ]
В роли донора электронов выступает убихинол QH2, который при этом окисляется до убихинона Q и в этом виде может возвращаться обратно и принимать следующую пару электронов и протонов. Убихинол передает электроны на цитохром, который транспортирует их в комплекс IV. Протонный насос комплекса III выбрасывает 4 протона в межмембранное пространство.
Комплекс IV [ править | править код ]
Электроны, поступившие от цитохрома с, передаются кислороду, и кислород полностью восстанавливается с образованием воды. Комплекс IV выбрасывает в межмембранное пространство только 2 протона.
АТФ-синтаза (комплекс V) [ править | править код ]
Этот комплекс состоит из «ножки гриба» — субъединицы F0, содержащей протонный канал, и из «выпуклой части» — АТФ-синтазы (или F1). Субъединица F0 получила свое название благодаря тому, что она ингибируется олигомицином, а субъединица F1 была первой открытой и выделенной «фракцией» среди всех элементов дыхательной цепи. Поток протонов проходит через протонный канал и запускает молекулярный двигатель, который заставляет АДФ и Фн реагировать друг с другом, образуя молекулы АТФ.
Чтобы синтезировать одну молекулу АТФ и транспортировать ее в цитозоль, требуется 4 протона. При окислении 1 молекулы НАДН+ высвобождается 10 протонов, энергия которых достаточно для образования 2,5 молекул АТФ. При окислении 1 молекулы ФАДН2 высвобождается 6 протонов, энергии которых достаточно для синтеза 1,5 молекул АТФ [1] .
Утечка электронов приводит к образованию активных форм кислорода [ править | править код ]
Примерно 2% электронов высвобождаются из дыхательной цепи и связываются непосредственно с кислородом, образуя активные формы кислорода (АФК). Если работа дыхательной цепи нарушена, АФК образуются в большем количестве. Эти вещества повреждают митохондрии, вызывая все большие нарушения дыхательной цепи. Возникает порочный круг, и в результате из-за накопления различных повреждений под действием АФК происходит старение клетки.
Дыхательные яды [ править | править код ]
Вещества, которые ингибируют образование АТФ, потенциально токсичны для организма.
Амитал и ротенон блокируют транспорт электронов в комплексе I. Ротенон выделяют из корней растения деррис (Derris scandens) и нередко используют в качестве природного пестицида. Он малотоксичен для человека, поскольку плохо всасывается в желудочно-кишечном тракте. Однако ротенон ядовит для рыб, так как быстро всасывается через жабры. К тому же при долговременном воздействии ротенон опасен и для человека, так как вызывает развитие болезни Паркинсона.
Антимицин блокирует транспорт электронов в комплексе III.
Цианиды(CN-), угарный газ (СО) и азиды (N3-) ингибируют комплекс IV. Поэтому при отравлении цианидом блокируются аэробные метаболические процессы, несмотря на то что кровь достаточно насыщена кислородом. Из-за остановки аэробного метаболизма венозная кровь принимает цвет артериальной крови. Кроме того, наблюдается гипервентиляция, поскольку из-за накопления молочной кислоты стимулируется дыхательный центр.
Олигомицин блокирует протонный канал (F0 в комплексе V) и не дает протонам возвращаться в матрикс. Поэтому АТФ-синтаза (F1) теряет способность синтезировать АТФ.
Биосинтез АТФ путем окислительного фосфорилирования (часть II) [ править | править код ]
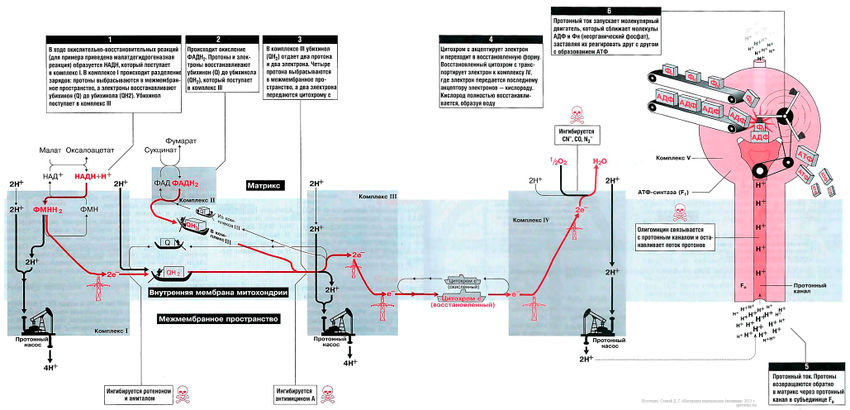
На рис. 13.1 показан поток электронов и протонов в дыхательной цепи. Электроны и протоны от НАДН+ через комплекс I и от ФАДН2 через комплекс II передаются комплексу III. Затем электроны транспортируются в комплекс IV, где они присоединяются к кислороду. В это время протоны выкачиваются протонными насосами из матрикса в межмембранное пространство и возвращаются обратно в матрикс через протонный канал F0-субъединицы АТФ-синтазы (комплекс V). Поток протонов (протонный ток) включает молекулярным двигатель — F1-субъединицу АТФ-синтазного комплекса, и она располагает молекулы АДФ и Фн таким образом, что они объединяются в молекулы АТФ.
АТФ (аденозинтрифосфат) строение, функции, гидролиз
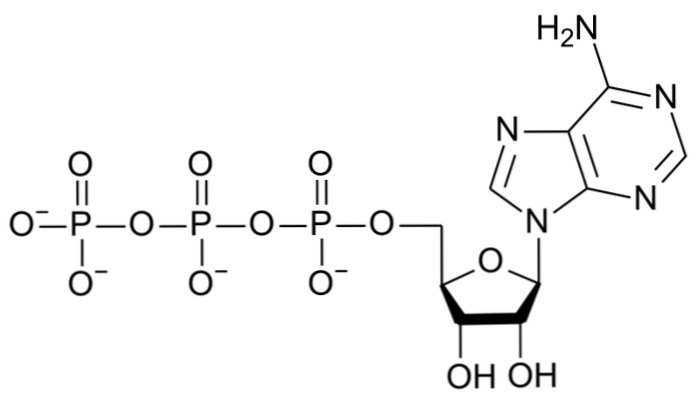
АТФ (аденозинтрифосфат) представляет собой органическую молекулу с высокоэнергетическими связями, состоящими из аденинового кольца, рибозы и трех фосфатных групп. Он играет фундаментальную роль в обмене веществ, так как он транспортирует необходимую энергию для эффективного функционирования ряда клеточных процессов..
Он широко известен под термином «энергетическая валюта», поскольку его образование и использование происходит легко, что позволяет быстро «оплачивать» химические реакции, требующие энергии..
Хотя молекула невооруженным глазом мала и проста, она сохраняет значительное количество энергии в своих звеньях. Фосфатные группы имеют отрицательные заряды, которые находятся в постоянном отталкивании, что делает его лабильным и легко разрушаемым звеном..
Гидролиз АТФ – это распад молекулы в присутствии воды. Благодаря этому процессу выделяемая энергия высвобождается.
Существует два основных источника АТФ: фосфорилирование на уровне субстрата и окислительное фосфорилирование, причем последний является наиболее важным и наиболее используемым клеткой..
Окислительное фосфорилирование сочетает окисление FADH2 и NADH + H + в митохондриях и фосфорилирования на уровне субстрата происходит вне цепи переноса электронов, в таких маршрутах, как гликолиз и цикл трикарбоновых кислот.
Эта молекула отвечает за обеспечение энергии, необходимой для большинства процессов, происходящих внутри клетки, от синтеза белка до локомоции. Кроме того, он обеспечивает прохождение молекул через мембраны и воздействует на передачу сигналов клетками..
- 1 структура
- 2 функции
- 2.1 Энергоснабжение для транспорта натрия и калия через мембрану
- 2.2 Участие в синтезе белка
- 2.3 Обеспечение энергией для передвижения
- 3 Гидролиз
- 3.1 Почему происходит это высвобождение энергии?
- 4 Получение АТФ
- 4.1 Окислительное фосфорилирование
- 4.2 Фосфорилирование на уровне субстрата
- 5 АТФ цикл
- 6 Другие энергетические молекулы
- 7 ссылок
структура
АТФ, как следует из его названия, является нуклеотидом с тремя фосфатами. Его особая структура, особенно две пирофосфатные связи, делают его энергетически богатым соединением. Он состоит из следующих элементов:
– Азотистое основание, аденин. Азотистые основания представляют собой циклические соединения, которые содержат в своей структуре один или несколько атомов азота. Мы также находим их в качестве компонентов в нуклеиновых кислотах, ДНК и РНК.
– Рибоза находится в центре молекулы. Это сахар пентозного типа, поскольку в нем пять атомов углерода. Его химическая формула C5H10О5. Углерод 1 рибозы присоединен к адениновому кольцу.
– Три фосфатных радикала. Последние два являются «звеньями высокой энергии» и представлены в графических структурах символом virgulilla:
. Фосфатная группа является одной из наиболее важных в биологических системах. Три группы называются альфа, бета и гамма, от ближайшего к дальнему.
Эта связь очень лабильна, поэтому она разделяется быстро, легко и спонтанно, когда этого требуют физиологические условия организма. Это происходит потому, что отрицательные заряды трех фосфатных групп пытаются постоянно отходить друг от друга..
функции
АТФ играет незаменимую роль в энергетическом обмене практически всех живых организмов. По этой причине его часто называют энергетической валютой, поскольку его можно постоянно тратить и пополнять всего за несколько минут..
Прямой или косвенный, АТФ обеспечивает энергию для сотен процессов, в дополнение к действию в качестве донора фосфата.
В общем, АТФ действует как сигнальная молекула в процессах, происходящих внутри клетки, необходимо синтезировать компоненты ДНК и РНК и для синтеза других биомолекул участвует в трафике через мембраны, среди других.
Использование АТФ можно разделить на основные категории: транспорт молекул через биологические мембраны, синтез различных соединений и, наконец, механическая работа..
Функции СПС очень широки. Кроме того, он вовлечен в так много реакций, что было бы невозможно назвать их всех. Поэтому мы обсудим три конкретных примера, иллюстрирующих каждое из трех упомянутых применений..
Энергоснабжение для транспорта натрия и калия через мембрану
Ячейка является чрезвычайно динамичной средой, которая требует поддержания определенных концентраций. Большинство молекул не попадают в клетку случайно или случайно. Для того чтобы молекула или вещество могли проникнуть внутрь, оно должно делать это посредством своего конкретного переносчика..
Транспортеры – это белки, которые пересекают мембрану и функционируют как клеточные «привратники», контролирующие поток материалов. Следовательно, мембрана является полупроницаемой: она позволяет некоторым соединениям проникать, а другим – нет..
Одним из самых известных видов транспорта является натриево-калиевый насос. Этот механизм классифицируется как активный транспорт, так как движение ионов происходит против их концентрации, и единственный способ выполнить это движение – ввести энергию в систему в форме АТФ..
Подсчитано, что одна треть АТФ, образующегося в клетке, используется для поддержания работы насоса. Ионы натрия постоянно перекачиваются на поверхность клетки, а ионы калия – наоборот.
Логично, что использование АТФ не ограничивается транспортировкой натрия и калия. Есть другие ионы, такие как кальций, магний и другие, которые нуждаются в этой энергетической валюте, чтобы войти.
Участие в синтезе белка
Молекулы белка образованы аминокислотами, связанными между собой пептидными связями. Для их формирования требуется разрыв четырех высокоэнергетических связей. Другими словами, для образования белка средней длины необходимо гидролизовать значительное количество молекул АТФ..
Синтез белков происходит в структурах, называемых рибосомами. Они способны интерпретировать код, которым обладает РНК-мессенджер, и транслировать его в аминокислотную последовательность, АТФ-зависимый процесс.
В наиболее активных клетках синтез белка может направлять до 75% АТФ, синтезированного в этой важной работе.
С другой стороны, клетка не только синтезирует белки, она также нуждается в липидах, холестерине и других необходимых веществах, и для этого требуется энергия, содержащаяся в связях АТФ..
Обеспечить энергию для передвижения
Механическая работа является одной из важнейших функций СПС. Например, чтобы наше тело могло выполнять сокращение мышечных волокон, необходимо наличие большого количества энергии..
В мышцах химическая энергия может быть преобразована в механическую энергию благодаря реорганизации протеинов с сокращающей способностью, которые ее формируют. Длина этих структур изменена, укорочена, что создает напряжение, которое приводит к генерации движения.
У других организмов движение клеток также происходит благодаря наличию АТФ. Например, движение ресничек и жгутиков, которое позволяет перемещать определенные одноклеточные организмы, происходит посредством использования АТФ.
Другое конкретное движение – амебное, которое включает в себя выпячивание псевдоподы на концах клетки. Несколько типов клеток используют этот механизм локомоции, включая лейкоциты и фибробласты.
В случае половых клеток локомоция необходима для эффективного развития эмбриона. Эмбриональные клетки перемещаются на значительные расстояния от места их происхождения до региона, в котором они должны создавать специфические структуры..
гидролиз
Гидролиз АТФ – это реакция, которая включает распад молекулы в присутствии воды. Реакция представляется следующим образом:
АТФ + Вода ⇋ АДФ + ПЯ + энергия. Где, термин PЯ оно относится к группе неорганических фосфатов, а ADP представляет собой аденозиндифосфат. Обратите внимание, что реакция обратима.
гидролиз АТФ это явление, которое включает высвобождение огромной энергии суммы. Разрывная любые ссылки пирофосфаты результаты в выпуске 7 ккал на моль – в частности 7.3 АТФ в АДФ и 8.2 для получения аденозин монофосфат (АМФ) из АТФ. Это соответствует 12000 калорий на моль АТФ.
Почему происходит это высвобождение энергии??
Поскольку продукты гидролиза намного более стабильны, чем исходное соединение, то есть АТФ.
Необходимо отметить, что только гидролиз, который происходит на пирофосфатных связях с образованием АДФ или АМФ, приводит к выработке энергии в важных количествах..
Гидролиз других связей в молекуле не обеспечивает столько энергии, за исключением гидролиза неорганического пирофосфата, который имеет большое количество энергии.
Выделение энергии из этих реакций используется для проведения метаболических реакций внутри клетки, поскольку многие из этих процессов требуют энергии для функционирования, как на начальных этапах путей деградации, так и в биосинтезе соединений..
Например, при метаболизме глюкозы начальные стадии включают фосфорилирование молекулы. На следующих шагах генерируется новый ATP, чтобы получить положительный чистый доход.
С энергетической точки зрения, существуют другие молекулы, у которых высвобождение энергии больше, чем у АТФ, включая 1,3-бифосфоглицерат, карбамилфосфат, креатининфосфат и фосфоенолпируват..
Получение АТФ
АТФ может быть получен двумя путями: окислительное фосфорилирование и фосфорилирование на уровне субстрата. Первый требует кислорода, а второй не нуждается в нем. Примерно 95% образовавшегося АТФ происходит в митохондриях.
Окислительное фосфорилирование
Окислительное фосфорилирование включает процесс окисления питательных веществ в две фазы: получение восстановленных коферментов NADH и FADH2 производные витаминов.
Восстановление этих молекул требует использования водорода из питательных веществ. У жиров выработка коэнзимов замечательна благодаря огромному количеству водородов, которые они имеют в своей структуре, по сравнению с пептидами или углеводами..
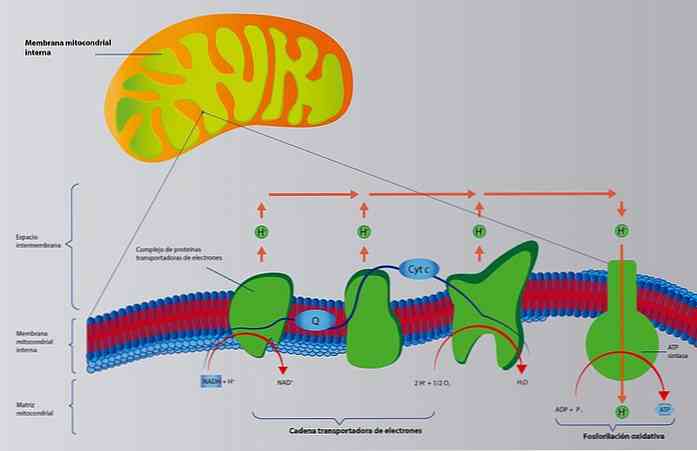
Хотя есть несколько способов получения коферментов, наиболее важный путь – цикл Кребса. Впоследствии восстановленные коферменты концентрируются в дыхательных цепях, расположенных в митохондриях, которые переносят электроны к кислороду.
Цепь переноса электронов образована серией белков, связанных с мембраной, которые накачивают протоны (H +) наружу (см. Изображение). Эти протоны снова проникают через мембрану через другой белок, АТФ-синтазу, отвечающую за синтез АТФ..
Другими словами, мы должны уменьшить коферменты, больше АДФ и кислорода вырабатывают воду и АТФ.
Фосфорилирование на уровне субстрата
Фосфорилирование на уровне субстрата не так важно, как механизм, описанный выше, и, поскольку оно не требует молекул кислорода, оно обычно связано с ферментацией. Таким образом, несмотря на то, что он очень быстрый, он извлекает мало энергии, если сравнить его с процессом окисления, он будет примерно в 15 раз меньше.
В нашем организме ферментативные процессы происходят на мышечном уровне. Эта ткань может функционировать без кислорода, поэтому вполне возможно, что молекула глюкозы разлагается до молочной кислоты (например, когда мы занимаемся спортом)..
В ферментации конечный продукт все еще обладает энергетическим потенциалом, который можно извлечь. В случае ферментации в мышцах содержание углерода в молочной кислоте находится на том же уровне восстановления, что и в исходной молекуле: глюкоза.
Таким образом, производство энергии происходит путем образования молекул, которые имеют высокоэнергетические связи, в том числе 1,3-бифосфоглират и фосфоенолпируват.
Например, в гликолизе гидролиз этих соединений связан с образованием молекул АТФ, отсюда и термин «на уровне субстрата»..
Цикл АТФ
АТФ никогда не сохраняется. Он находится в непрерывном цикле использования и синтеза. Таким образом, создается баланс между образованным АТФ и его гидролизованным продуктом, АДФ..
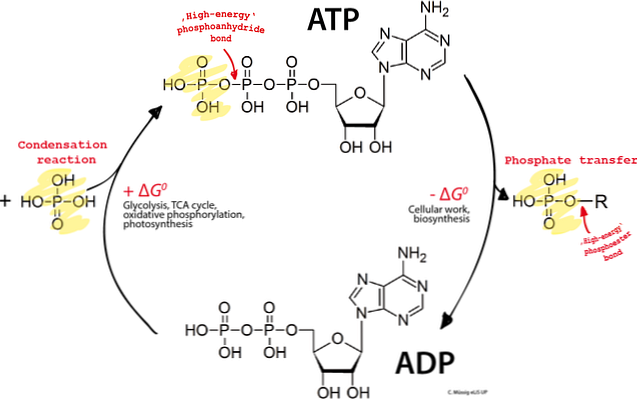
Другие энергетические молекулы
АТФ не единственная молекула, состоящая из нуклеозид-бифосфата, который существует в клеточном метаболизме. Существует ряд молекул со структурами, похожими на АТФ, которые имеют сравнимое энергетическое поведение, хотя они не так популярны, как АТФ.
Наиболее ярким примером является ГТФ, трифосфат гуанозина, который используется в известном цикле Кребса и в глюконеогенном пути. Другие менее используемые CTP, TTP и UTP.
Синтез АТФ — структура, функции и пути образования аденозинтрифосфорной кислоты
Синтез АТФ – процесс, направленный на поддержание жизнедеятельности клетки, сопровождаемый образованием энергии. Образование АТФ происходит на внутренней мембране митохондрий, которые являются энергетическим аккумулятором клетки.
Расшифровка АТФ
Аденозинтрифосфорная кислота или АТФ – необходимое условие для существования 9 из 10 клеток с аэробным дыханием. Получение энергии происходит при фосфорилировании, присоединении остатка фосфорной кислоты. На одну молекулу АТФ приходится около 7,3 килокалории энергии.

Какие соединения входят в состав АТФ
Строение АТФ и биологическая роль тесно связаны. В состав АТФ входят аденозин, три остатка фосфорной кислоты. Связи, существующие между аминокислотой и фосфатом, подвергаются гидролизу в присутствии воды, в результате образуется АДФ (аденозиндифосфат), фосфорная кислота. Этот процесс происходит с высвобождением энергии.

Энергообразование происходит за счет разрыва макроэргических связей АТФ (обозначаемых в формуле знаком тильда). Сам аденозин состоит из аденина – пуринового нуклеотида и рибозы. Первая участвует в синтезе ДНК, вторая — составляющая структуры РНК.
Образование энергии
Макроэргическая связь заключена между общими электронами остатков фосфорной кислоты (что и удерживает их вместе). Кислород и фосфор образуют общую электронную пару — высокоэнергетическую. Поэтому при отщеплении снижается энергия электронов: отщепляется фосфат и выделяется ее избыточное количество.

Процесс переноса электронов осуществляется посредством дыхательной цепи. Основную роль здесь играет восстановленный НАДН (Никотинамидадениндинуклеотид). Данное вещество окисляется, отдавая водород. Также на дыхательной цепи синтезируется АТФ. Фосфорилирование происходит на внутренней стороне мембраны митохондрии при помощи АТФ-синтазы.
Последняя выступает переносчиком ионов водорода, что необходимо в связи с существованием градиента на внутренней и внешней мембранах. Перенос водорода через мембрану – хемиосмос, ведет к возникновению связи между АДФ и остатком фосфорной кислоты, иначе говоря, к окислительному фосфорилированию.
Пути синтеза АТФ и его роль
Образование АТФ возможно в ходе гликолиза, цикла трикарбоновых кислот или цикла Кребса. Такие процессы носят название субстратного фосфорилирования.

В ходе первого получают четыре молекулы АТФ, две молекулы пирувата или пировиноградной кислоты из глюкозы. Это бескислородное расщепление. На обеспечение данного процесса затрачивается 2 АТФ, протекает он в цитоплазме или цитозоле. Цикл лимонной кислоты происходит на кристах (складки внутренней оболочки) митохондрий в ходе окисления пирувата. При этом происходит отщепление одного атома углерода с образованием ацетилкоэнзима А и восстановление НАДН.
Далее синтезируется лимонная кислота при участии щавелевоуксусной кислоты. Цитрат превращается в цис-аконитат, который переходит в изоцитрат. К последнему присоединяется окисленный НАДН, который восстанавливается. Отщепление водорода приводит к синтезу кетоглутарата, с ним снова соединяется окисленный НАДН и ацетилкоэнзим А. На этой стадии синтезируется сукцинил-коэнзим А, к которому присоединяется ГДФ (гуанозиндифосфат).
Данная молекула восстанавливается в ГТФ (гуанозинтрифосфат) плюс образуется сукцинат. Он превращается в фумарат, затем малат. В этой реакции синтезируется оксалоацетат и восстановленный НАДН. Так, цикл Кребса возвращается к цитрату. На каждый цикл затрачиваются 2 молекулы АТФ, синтезируется 6 НАДН в цикле и 4 на подготовительных этапах. Последняя энергетически приравнивается к трем молекулам АТФ.
В синтезе цитрата задействованы также два ФАДН2 (флавинадениндинуклеотид), на каждую приходится по две АТФ. Таким образом, синтезируемое количество АТФ соответствует 38 молекулам с позиций биологии и биохимии. Однако следует помнить, что это теоретическое число, необходимое для дыхания клетки. Все реакции цикла Кребса катализируются ферментами.
Главная роль – поддержание клеточного дыхания, направленного на рост клетки, синтез новых веществ.
Функции АТФ
Важнейшая функция – участие в энергетическом обмене. Энергия, выделяемая в ходе данных превращений, вновь идет на синтез АТФ. При этом 40% рассеивается в виде тепла.

Поскольку для поддержания любых процессов жизнедеятельности необходимы энергозатраты АТФ – аккумулятор клетки, универсальный источник запасов энергии. Гликолиз активно протекает при физической нагрузке, в мышцах. Субстратное фосфорилирование также осуществляется из креатинфосфата других органических веществ.
Важно подчеркнуть, что цикл Кребса протекает при расщеплении как углеводов, так и белков и жиров. Если в качестве «топлива» клетка использует не углевод, гликолиз не протекает (отсюда не происходит затрата двух молекул АТФ с образованием четырех). Но цикл трикарбоновых кислот протекает одинаково, так как главную роль там играет ацетил-коэнзим А. При кислородном голодании клетка перестраивается на гликолитический путь.
Заключение
АТФ — это особое соединение, содержащее связи, при гидролизе которых высвобождается огромное количество энергии. Называя синтезом АТФ процесс, выполняющий функцию поддержания жизнедеятельности клетки, нельзя не понять, каково значение этого явления. В действительности количество синтезируемого аденозинтрифосфата может быть меньше 38 молекул. Суть процесса заключается в синтезе макроэргических веществ, поступающих в дыхательную цепь переноса электронов.
Аденозинтрифосфорная кислота
Строение, химические свойства аденозинтрифосфорной кислоты (АТФ). Роль АТФ в организме. Осуществление активного переноса молекул через биологические мембраны. Создание трансмембранного электрического потенциала. Осуществление мышечного сокращения.
| Рубрика | Биология и естествознание |
| Вид | реферат |
| Язык | русский |
| Дата добавления | 11.11.2017 |
| Размер файла | 13,9 K |
- посмотреть текст работы
- скачать работу можно здесь
- полная информация о работе
- весь список подобных работ

Отправить свою хорошую работу в базу знаний просто. Используйте форму, расположенную ниже
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Размещено на http://www.allbest.ru/
Каждое живое существо – это сложная биологическая система, работа и функционирование которой обеспечивает стабильную и нормальную жизнь каждому.
АТФ – Аденозинтрифосфат – (аденозинтрифосфорная кислота) — это универсальный источник энергии для всех живых клеток, который питает биологические реакции, обеспечивает связь между клетками и тканями организма.
Аденозинтрифосфорная кислота (АТФ) состоит из азотистого основания аденина , углевода рибозы (относящейся к группе пентоз) и трех остатков фосфорной кислоты. Соединение аденина и рибозы называется аденозином. Пирофосфатные группы имеют макроэргические связи. К рибозе может присоединиться максимально три остатка фосфорной кислоты. Если их два или только один, то соответственно вещество называется АДФ (дифосфат) или АМФ (монофосфат). Именно между фосфорными остатками заключены макроэнергетические связи.
Химически АТФ – это трифосфорный эфир аденозина. АТФ относится к макроэргическим соединениям, особенность которых — высвобождение значительного количества энергии при гидролизе. Эта высвобождающаяся энергия впоследствии участвует с самых разных процессах, которые требуют любых энергозатрат.
Разложение одной молекулы АТФ с участием воды сопровождается отщеплением одной молекулы фосфорной кислоты и выделением свободной энергии, которая равна 33–42 кДж/моль. Все реакции с участием АТФ регулируются ферментными системами.
аденозинтрифосфорный кислота молекула биологический
Главная роль АТФ в организме связана с обеспечением энергией многочисленных биохимических реакций. Являясь носителем двух высокоэнергетических связей, АТФ служит непосредственным источником энергии для множества энергозатратных биохимических и физиологических процессов. Все это реакции синтеза сложных веществ в организме: осуществление активного переноса молекул через биологические мембраны, в том числе и для создания трансмембранного электрического потенциала; осуществления мышечного сокращения.
Помимо энергетической АТФ выполняет в организме ещё ряд других не менее важных функций:
· Вместе с другими нуклеозидтрифосфатами АТФ является исходным продуктом при синтезе нуклеиновых кислот.
· Кроме того, АТФ отводится важное место в регуляции множества биохимических процессов. Являясь аллостерическим эффектором ряда ферментов, АТФ, присоединяясь к их регуляторным центрам, усиливаетили подавляет их активность.
· АТФ является также непосредственным предшественником синтеза циклического аденозинмонофосфата –вторичного посредника передачи в клетку гормонального сигнала.
· Также известна роль АТФ в качестве медиатора в синапсах.
· Не последнюю роль АТФ играет и в метаболизме.
Метаболизм – это совокупность химических реакций, протекающих во внутренней среде организма, т.е. в его клетках. В свою очередь, метаболизм делится на катаболизм и анаболизм. В процессе катаболизма освобождается энергия, примерно половина которой аккумулируется в форме химической энергии аденозинтрифосфата (АТФ). Другая часть энергии выделяется в виде тепла.
Анаболизм протекает с потреблением энергии, источником которой является АТФ.
Одновременное протекание реакций катаболизма и анаболизма приводит к обновлению химического состава организма, что является обязательным условием его жизнедеятельности.
Строение АТФ и биологическая роль его молекул тесно связаны. Вещество играет ключевую роль в процессах жизнедеятельности, ведь в макроэргических связях между фосфатными остатками содержится огромное количество энергии. Аденозинтрифосфат выполняет множество функций в клетке, и поэтому важно поддерживать постоянную концентрацию вещества. Распад и синтез идут с большой скоростью, т. к. энергия связей постоянно используется в биохимических реакциях. Это незаменимое вещество любой клетки организма.
Размещено на Allbest.ru
Подобные документы
Особенности строения клеток прокариот и эукариот. Структура фосфолипидного бислоя. Связи в молекуле фосфолипида, расщепляемые разными классами фосфолипаз. Липидный состав плазматической мембраны. Обзор основных способов переноса веществ через мембраны.
презентация [8,1 M], добавлен 26.03.2015
Понятие и функциональные особенности в организме витамина С как единственного активного изомера аскорбиновой кислоты (L-аскорбиновая кислота). Его содержание в различных овощах и фруктах, степень усвояемости. Реакции гидроксилирования. Причины цинги.
презентация [1,9 M], добавлен 18.03.2014
Проблемы объяснения механизмов йоги с точки зрения физиологии. Процессы сокращения и расслабления мышечного волокна. Энергетическая валюта организма – аденозинтрифосфорная кислота (АТФ). Взаимосвязь скелетной мускулатуры с центральной нервной системой.
реферат [15,4 K], добавлен 14.11.2010
Строение мембран. Мембраны эритроцитов. Миелиновые мембраны. Мембраны хлоропластов. Внутренняя (цитоплазматическая) мембрана бактерий. Мембрана вирусов. Функции мембран. Транспорт через мембраны. Пассивный транспорт. Активный транспорт. Ca2+ –насос.
реферат [18,2 K], добавлен 22.03.2002
Первичная, вторичная и третичная структуры ДНК. Свойства генетического кода. История открытия нуклеиновых кислот, их биохимические и физико-химические свойства. Матричная, рибосомальная, транспортная РНК. Процесс репликации, транскрипции и трансляции.
реферат [4,1 M], добавлен 19.05.2015
Преобразование химической энергии в механическую работу или силу как основная функции мышц, их механические свойства. Применение закона Гука в отношении малых напряжений и деформаций. Механизм мышечного сокращения. Ферментативные свойства актомиозина.
презентация [3,0 M], добавлен 23.02.2013
Нуклеиновые кислоты, их структура, функциональные группы. Осмотическое давление различных клеток и тканей растения. Роль пигментов в жизни растений. Биосинтез углеводов, ферменты углеводного обмена. Роль аденозинтрифосфорной кислоты в обмене веществ.
контрольная работа [843,8 K], добавлен 12.07.2010
Биология. 11 класс
§ 8. Строение и функции РНК. АТФ
Строение и функции РНК. РНК, так же как и ДНК, представляет собой биополимер, построенный из нуклеотидов. Однако молекулы РНК имеют ряд особенностей. Вы знаете, что в состав нуклеотидов РНК вместо дезоксирибозы входит рибоза, а вместо тимина (Т) — урацил (У). Кроме того, молекулы РНК значительно короче ДНК и представлены одной полинуклеотидной цепью, а не двумя.
Лишь некоторые вирусы имеют двухцепочечные молекулы РНК, представляющие собой генетический материал этих неклеточных форм.
*Количество нуклеотидов в молекулах ДНК, как правило, исчисляется миллионами, в то время как полинуклеотидные цепи РНК обычно состоят из 75—3000 мономерных звеньев. Известно, что некоторые РНК могут включать десятки тысяч нуклеотидов, но это является не правилом, а исключением.*
Молекулы РНК могут принимать различную пространственную конфигурацию, прежде всего за счет образования водородных связей. Но, в отличие от ДНК, эти связи формируются не между двумя разными цепями, а между отдельными участками одной и той же цепи, комплементарными друг другу.
*Содержание ДНК в клетках организма сравнительно постоянно, а количество РНК сильно варьирует. Молекулы РНК обеспечивают синтез белков, поэтому наибольшее их содержание характерно для клеток, активно вырабатывающих белки. Это, например, секреторные клетки пищеварительных и эндокринных желез, синтезирующие ферменты и белковые гормоны, лейкоциты, продуцирующие антитела, и т. д.*
Существует несколько видов РНК, различающихся по строению молекул, содержанию в клетке и выполняемым функциям. Все виды РНК синтезируются на определенных участках одной из цепей ДНК. Такой синтез называется матричным, поскольку молекула ДНК является матрицей (т. е. образцом, моделью) для построения молекул РНК.
Рибосомные РНК (рРНК) составляют более 80 % всех РНК клетки. Молекулы рРНК соединяются с особыми белками и образуют рибосомы — органоиды, в которых происходит синтез белков из аминокислот.
*Молекулы рРНК составляют более 50 % массы рибосомы и имеют сложную объемную структуру. Бóльшую часть цепи рРНК составляют комплементарные участки. Они соединяются водородными связями и приобретают спиральную конфигурацию. Взаимодействуя с рибосомными белками, одна или несколько молекул рРНК компактно укладываются в пространстве. Так формируются субъединицы рибосом — структурные компоненты этих органоидов.
Установлено, что рРНК в составе рибосомы выполняют не только структурную функцию, но и каталитическую. В процессе синтеза белка они ускоряют образование пептидных связей между аминокислотами, т. е. действуют подобно ферментам. Такие молекулы РНК, обладающие каталитическим действием, были названы рибозимами (сокращение от «рибонуклеиновая кислота» и «энзим»). Кроме рРНК, известны и другие рибозимы. Они могут катализировать расщепление самих себя или других молекул РНК, а также соединять фрагменты РНК друг с другом.
До открытия рибозимов единственными биологическими катализаторами считались ферменты. За исследование каталитических свойств рибонуклеиновых кислот американские молекулярные биологи С. Олтмен и Т. Чек в 1989 г. были награждены Нобелевской премией.*
Транспортные РНК (тРНК) — самые маленькие из молекул РНК, участвующих в синтезе белков. В среднем они состоят из 80 нуклеотидов. тРНК связывают аминокислоты, доставляют их в рибосомы и обеспечивают правильное включение этих аминокислот в полипептидную цепь. Для каждой из 20 белокобразующих аминокислот существует как минимум одна особая разновидность тРНК, а для некоторых аминокислот — несколько. Содержание тРНК составляет около 15 % от общего количества клеточных РНК.
Все тРНК имеют сходное строение. Благодаря образованию внутримолекулярных водородных связей молекулы тРНК приобретают особую структуру, в которой комплементарно связанные участки чередуются с петлями (рис. 8.1). Такая пространственная конфигурация была названа клеверным листом.
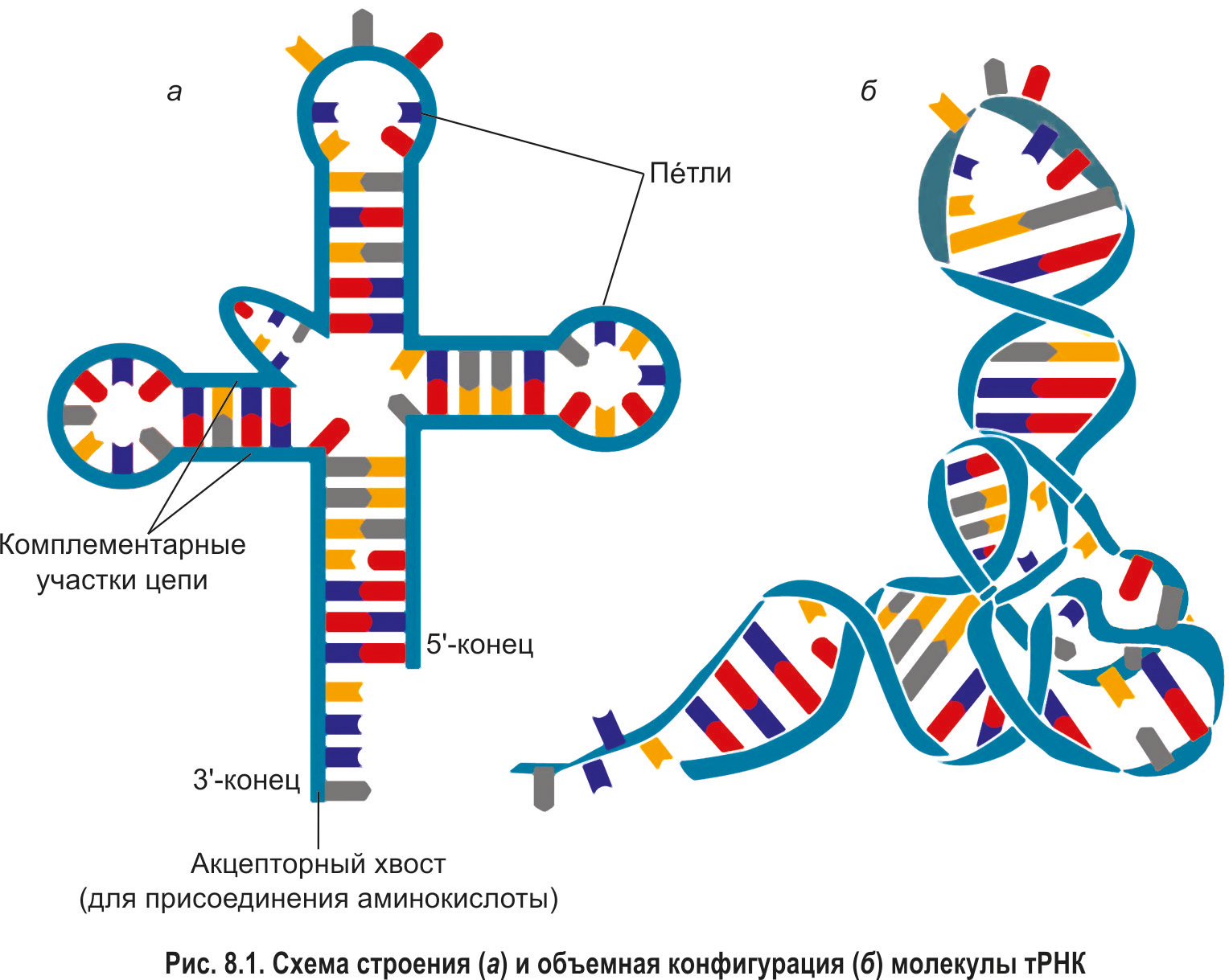
*Как и любая другая полинуклеотидная цепь, молекула тРНК имеет 5′- и 3′-концы. У всех тРНК на 5′-конце находится гуаниловый нуклеотид, а 3′-конец завершается последовательностью ЦЦА. Присоединение аминокислоты происходит именно к 3′-концу молекулы тРНК, поэтому он называется акцепторным хвостом.*
Матричные, или информационные, РНК (мРНК, иРНК) наиболее разнообразны по строению и длине цепей. Молекулы мРНК содержат информацию о первичной структуре определенных белков. Во время синтеза белков в рибосомах они служат матрицами, определяющими порядок расположения аминокислот в белковых молекулах. Поэтому биосинтез белка, так же как и синтез РНК, относится к матричным процессам. Количество мРНК не превышает 3—5 % всех РНК, содержащихся в клетке.
*У ядерных организмов каждая молекула мРНК, как правило, содержит закодированную информацию о структуре одного белка. Для бактерий и вирусов характерны мРНК, кодирующие несколько разных белков.*
Функции рассмотренных видов РНК связаны с процессами синтеза белка. Следовательно, рРНК, тРНК и мРНК обеспечивают реализацию наследственной информации, хранящейся в молекулах ДНК.
Молекула АТФ в биологии: состав, функции и роль в организме
 Важнейшим веществом в клетках живых организмов является аденозинтрифосфорная кислота или аденозинтрифосфат. Если ввести аббревиатуру этого названия, то получим АТФ (англ. ATP). Это вещество относится к группе нуклеозидтрифосфатов и играет ведущую роль в процессах метаболизма в живых клетках, являясь для них незаменимым источником энергии.
Важнейшим веществом в клетках живых организмов является аденозинтрифосфорная кислота или аденозинтрифосфат. Если ввести аббревиатуру этого названия, то получим АТФ (англ. ATP). Это вещество относится к группе нуклеозидтрифосфатов и играет ведущую роль в процессах метаболизма в живых клетках, являясь для них незаменимым источником энергии.
Первооткрывателями АТФ стали учёные-биохимики гарвардской школы тропической медицины — Йеллапрагада Суббарао, Карл Ломан и Сайрус Фиске. Открытие произошло в 1929 году и стало главной вехой в биологии живых систем. Позднее, в 1941 году, немецким биохимиком Фрицем Липманом было установлено, что АТФ в клетках является основным переносчиком энергии.
Строение АТФ
Эта молекула имеет систематическое наименование, которое записывается так: 9-β-D-рибофуранозиладенин-5-трифосфат, или 9-β-D-рибофуранозил-6-амино-пурин-5-трифосфат. Какие соединения входят в состав АТФ? Химически она представляет собой трифосфорный эфир аденозина — производного аденина и рибозы. Это вещество образуется путём соединения аденина, являющегося пуриновым азотистым основанием, с 1-углеродом рибозы при помощи β-N-гликозидной связи. К 5-углероду рибозы затем последовательно присоединяются α-, β- и γ-молекулы фосфорной кислоты.
 Таким образом, молекула АТФ содержит такие соединения, как аденин, рибозу и три остатка фосфорной кислоты. АТФ — это особое соединение, содержащее связи, при гидролизе которых высвобождается большое количество энергии. Такие связи и вещества называются макроэргическими. Во время гидролиза этих связей молекулы АТФ происходит выделение количества энергии от 40 до 60 кДж/моль, при этом данный процесс сопровождается отщеплением одного или двух остатков фосфорной кислоты.
Таким образом, молекула АТФ содержит такие соединения, как аденин, рибозу и три остатка фосфорной кислоты. АТФ — это особое соединение, содержащее связи, при гидролизе которых высвобождается большое количество энергии. Такие связи и вещества называются макроэргическими. Во время гидролиза этих связей молекулы АТФ происходит выделение количества энергии от 40 до 60 кДж/моль, при этом данный процесс сопровождается отщеплением одного или двух остатков фосфорной кислоты.
Вот как записываются эти химические реакции:
- 1). АТФ + вода→АДФ + фосфорная кислота + энергия,
- 2). АДФ + вода→АМФ + фосфорная кислота + энергия.
Энергия, высвобожденная в ходе указанных реакций, используется в дальнейших биохимических процессах, требующих определённых энергозатрат.
Роль АТФ в живом организме. Её функции
Какую функцию выполняет АТФ? Прежде всего, энергетическую. Как уже было выше сказано, основной ролью аденозинтрифосфата является энергообеспечение биохимических процессов в живом организме. Такая роль обусловлена тем, что благодаря наличию двух высокоэнергетических связей, АТФ выступает источником энергии для многих физиологических и биохимических процессов, требующих больших энергозатрат. Такими процессами являются все реакции синтеза сложных веществ в организме. Это, прежде всего, активный перенос молекул через клеточные мембраны, включая участие в создании межмембранного электрического потенциала, и осуществление сокращения мышц.
Кроме указанной, перечислим ещё несколько, не менее важных, функций АТФ, таких, как:
 медиатор в синапсах и сигнальное вещество в других межклеточных взаимодействиях (функция пуринергической передачи сигнала),
медиатор в синапсах и сигнальное вещество в других межклеточных взаимодействиях (функция пуринергической передачи сигнала),- регуляция различных биохимических процессов, таких, как усиление или подавление активности ряда ферментов путём присоединения к их регуляторным центрам (функция аллостерического эффектора),
- участие в синтезе циклического аденозинмонофосфата (АМФ), являющегося вторичным посредником в процессе передачи гормонального сигнала в клетку (в качестве непосредственного предшественника в цепочке синтеза АМФ),
- участие вместе с другими нуклеозидтрифосфатами в синтезе нуклеиновых кислот (в качестве исходного продукта).
Как образуется АТФ в организме?
Синтез аденозинтрифосфорной кислоты идёт постоянно, т. к. энергия организму для нормальной жизнедеятельности нужна всегда. В каждый конкретный момент содержится совсем немного этого вещества — примерно 250 граммов, которые являются «неприкосновенным запасом» на «чёрный день». Во время болезни идёт интенсивный синтез этой кислоты, потому что требуется много энергии для работы иммунной и выделительной систем, а также системы терморегуляции организма, что необходимо для эффективной борьбы с начавшимся недугом.
В каких клетках АТФ больше всего? Это клетки мышечной и нервной тканей, поскольку в них наиболее интенсивно идут процессы энергообмена. И это очевидно, ведь мышцы участвуют в движении, требующем сокращения мышечных волокон, а нейроны передают электрические импульсы, без которых невозможна работа всех систем организма. Поэтому так важно для клетки поддерживать неизменный и высокий уровень аденозинтрифосфата.
Каким же образом в организме могут образовываться молекулы аденозинтрифосфата? Они образуются путём так называемого фосфорилирования АДФ (аденозиндифосфата). Эта химическая реакция выглядит следующим образом:
АДФ + фосфорная кислота + энергия→АТФ + вода.
Фосфорилирование же АДФ происходит при участии таких катализаторов, как ферменты и свет, и осуществляется одним из трёх способов:
 фотофосфорилирование (фотосинтез у растений) ,
фотофосфорилирование (фотосинтез у растений) ,- окислительное фосфорилирование АДФ Н-зависимой АТФ-синтáзой, в результате которого основная масса аденозинтрифосфата образуется на мембранах митохондрий клеток (связано с дыханием клетки),
- субстратное фосфорилирование в цитоплазме клетки в процессе гликолиза или путём переноса фосфатной группы с других макроэргических соединений, не требующее участия мембранных ферментов.
Как окислительное, так и субстратное фосфорилирование использует энергию веществ, окисляющихся в процессе такого синтеза.
Вывод
Аденозинтрифосфорная кислота — это наиболее часто обновляемое вещество в организме. Сколько в среднем живёт молекула аденозинтрифосфата? В теле человека, например, продолжительность её жизни составляет менее одной минуты, поэтому одна молекула такого вещества рождается и распадается до 3000 раз за сутки. Поразительно, но в течение дня человеческий организм синтезирует около 40 кг этого вещества! Настолько велики потребности в этом «внутреннем энергетике» для нас!
Весь цикл синтеза и дальнейшего использования АТФ в качестве энергетического топлива для процессов обмена веществ в организме живого существа представляет собой саму суть энергетического обмена в этом организме. Таким образом, аденозинтрифосфат является своего рода «батарейкой», обеспечивающей нормальную жизнедеятельность всех клеток живого организма.
 медиатор в синапсах и сигнальное вещество в других межклеточных взаимодействиях (функция пуринергической передачи сигнала),
медиатор в синапсах и сигнальное вещество в других межклеточных взаимодействиях (функция пуринергической передачи сигнала), фотофосфорилирование (фотосинтез у растений) ,
фотофосфорилирование (фотосинтез у растений) ,




